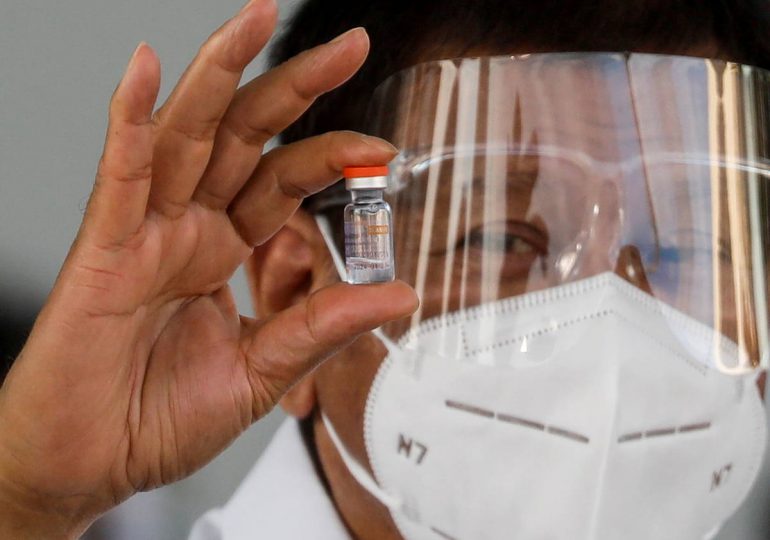
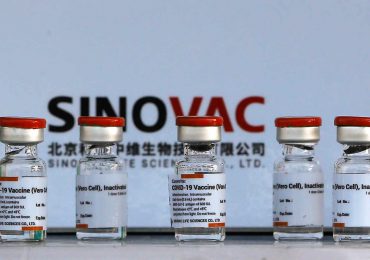
AFP.- La Agencia Europea de Medicamentos (EMA) anunció este martes que inició un “examen continuo” de la vacuna china Sinovac contra el covid-19, lo que allana el camino para una futura autorización en la Unión Europea (UE).
La decisión del Comité de Medicamentos de la EMA de “comenzar el examen continuo se basa en los resultados previos de estudios de laboratorio y estudios clínicos”, dijo la agencia con sede en Ámsterdam en un comunicado.
La vacuna del laboratorio chino Sinovac utiliza la técnica del virus inactivado que ayuda a la persona vacunada a producir anticuerpos contra el virus.
“Estos estudios sugieren que la vacuna provoca la producción de anticuerpos que se dirigen hacia el SARS-CoV-2, virus que causa el covid-19, y puede ayudar a la protección contra la enfermedad”, indicó la EMA.
La agencia europea continuará la revisión hasta contar con suficiente información para que la empresa pueda presentar una solicitud formal para su lanzamiento en el mercado.
“A pesar de que la EMA no puede prever los plazos, debería llevar menos tiempo que lo normal evaluar una eventual aplicación como consecuencia del trabajo realizado durante la revisión continua”, indicó.
La vacuna de Sinovac fue autorizada en febrero en China y también en Chile, Brasil, Filipinas, Ucrania y Turquía, entre otros.
Actualmente cuatro vacunas están autorizadas en la UE: Pfizer-BioNTech, Moderna, AstraZeneca y Johnson & Johnson, las dos últimas dependiendo de ciertas condiciones vinculadas a la edad en la mayoría de países europeos.
La Sinovac china se utiliza por lo menos 22 países y territorios (de los 209 que comenzaron a vacunar), lo que incluye a varios países de América Latina, África y Asia, según un recuento de la AFP.
Es menos que las dos vacunas chinas desarrolladas por Sinopharm, usadas por 42 países, incluido Hungría en la UE.
La vacuna AstraZeneca se utiliza en al menos 165 sobre 209 países y territorios que están inoculando, la Pfizer/BioNTech en al menos 94, y Moderna en al menos 46, también según un recuento de la AFP.